Химия - Активность (химия)
06 мая 2011Оглавление:
1. Активность (химия)
2. Выбор стандартного состояния
3. Методы определения активности
Активность компонентов раствора — эффективная концентрация компонентов с учетом различных взаимодействий между ними в растворе, то есть с учетом отклонения поведения системы от модели идеального раствора.
Активность была предложена в 1907 году Льюисом как новая переменная, применение которой вместо концентрации позволяет использовать для описания свойств реальных растворов относительно простые уравнения, полученные для идеальных систем. Альтернативой этому пути является использование более сложных уравнений, учитывающих взаимодействие между частицами.
Активность отличается от общей концентрации на некоторую величину. Отношение активности к общей концентрации вещества в растворе называется коэффициентом активности:
Коэффициент активности служит мерой отклонения поведения раствора от идеального. Отклонения от идеальности могут быть обусловлены различными химическими и физическими причинами — дипольные взаимодействия, поляризация, образование водородных связей, ассоциация, диссоциация, сольватация и др.
Исходя из понятия химического потенциала, активность компонента в растворе можно определить как величину, которую нужно подставить в выражения для химического потенциала компонента в идеальном растворе:
вместо мольной доли x, для того, чтобы получить действительное значение химического потенциала  -го компонента в реальном растворе:
-го компонента в реальном растворе:
где 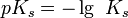 — стандартный химический потенциал.
— стандартный химический потенциал.
Размерность и величина активности зависит от используемого способа выражения концентрации — если 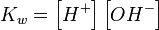 величина безразмерная, то
величина безразмерная, то 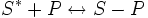 и
и 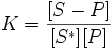 — размерные величины, выражаются в моль/л и моль/кг.
— размерные величины, выражаются в моль/л и моль/кг.
Коэффициент активности в общем случае может быть как больше, так и меньше единицы. Возможны и знакопеременные отклонения от идеального поведения. Так, например, для железа в системе Fe-S при 1300 °C в рекомендуются коэффициенты активности от 0,004 при 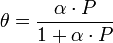 до 1,47 при
до 1,47 при 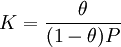 .
.
Отметим, что величина активности и коэффициента активности может быть различной в зависимости от выбора стандартного состояния.
Просмотров: 6785
|
|