Химия - Фосфиты
28 февраля 2011Оглавление:
1. Фосфиты
2. Кислые фосфиты
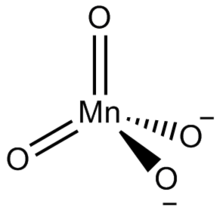
соли фосфористой кислоты Н3РО3. Анион фосфористой кислоты является многоатомным ионом, в котором центральным атомом является атом фосфора в степени окисления +3. Его молекулярная геометрия приблизительно тетраэдрическая.
Связывание может быть объяснено с помощью резонансных структур, эффективно делокализующих отрицательные заряды между эквивалентными атомами кислорода.
Множество солей фосфористой кислоты, такие как фосфит аммония, очень хорошо растворимы в воде. Иногда название фосфиты относят также к эфирам этой кислоты, фосфорорганическим соединениям с формулой P3.
-
 Структура типичного фосфита.
Структура типичного фосфита.
Фосфористая кислота
Фосфористая кислота является сопряженной кислотой фосфит-аниона2). Также эта кислота называется ортофосфористой или оксидом дигидроксифосфина. Фосфористая кислота является двухосновной кислотой, так как один из атомов водорода связан напрямую с центральным атомом фосфора и не может быть ионизирован. Таким образом более логичной химической формулой будет HPO2, так как только две гидроксильных группы действительно присутствуют в молекуле кислоты.
Просмотров: 2356
|
|