Химия - Галогенуглеводороды - Получение
28 февраля 2011Оглавление:
1. Галогенуглеводороды
2. Физические свойства
3. Получение
4. Химические свойства
При синтезе галогеналканов обычно исходят из углеводородов, спиртов или карбоновых кислот.
Получение галогеналканов
Прямое галогенирование
Радикальным галогенированием можно получать хлор- или бромалканы. Недостатком этого метода является то, что образуется смесь различных продуктов замещения. При этом наряду с изомерными монозамещёнными в смеси также содержатся ди- и полизамещённые соединения. К тому же, например, эквимолярная смесь Cl2 и CH4 взрывоопасна, не говоря уже о смесях алканов со фтором. Однако меняя условия процесса можно добиться приемлемых для промышленности выходов. Например, при хлорировании алкан берут в избытке. Продукты разделяют фракционной перегонкой. К примеру, так в промышленности получают метиленхлорид и тетрахлоруглерод.
Алканы хлорируются при интенсивном УФ-облучении или нагревании. Наиболее легко образуются третичные радикалы и, соответственно, галогеналканы; наименее – первичные. Бромирование мало характерно для алканов легче гексана, а прочие бромируются при одновременном освещении и кипячении.
CnH2n+2 + X2 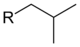 CnH2n+1X + HX
CnH2n+1X + HX 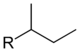 CnH2nX2 + HX
CnH2nX2 + HX  ...
...
В присутствии специальных реагентов, а также инициаторов свободных радикалов замещённые алкены бромируются в аллильное положение.
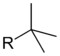
Аллильное хлорирование осуществляется лишь при 400–600°C, обычно же идут конкурирующие реакции – присоединение по двойной связи, полимеризация, изомеризация алкенов. В промышленности так производят аллилхлорид.
Замещённые арены хлорируются и бромируются в боковую цепь. Например, толуол при нагревании и интенсивном освещении хлорируют, получая бензилхлорид.
Радикальным методом получают также и перфторалканы. Реакция протекает очень энергично, и вследствие большого тепловыделения приходится разбавлять фтор азотом, применяют также медные сетки для отвода теплоты. В процессе применяют переносчики фтора – фториды металлов, как CoF2, MnF2, AgF, образующие в ходе реакции соответственно CoF3, MnF4, AgF2.
Получение моногалогеналканов
- Присоединение галогеноводородов к алкенам.
R-CH=CH2+HCl→R-CHCl-CH3
- Весьма легко присоединяется фтор, иод присоединяется медленно. Обычно происходит стереоселективно, кроме как в присутствии свободных радикалов. В присутствии других нуклеофилов возможно сопряжённое присоединение.
- Реакции спиртов с галогеноводородами.
R-OH+H-Cl→R-Cl+H2O - Взаимодействие галогенидов фосфора или тионилхлорида со спиртами.
3R-OH+PCl3→3R-Cl+H3PO3 - Реакция Бородина — Хунсдикера

- Реакция Сварта
R-Cl+AgF→R-F+AgCl
Получение дигалогеналканов
- Присоединение галогеноводородов к алкинам.
R-C≡CH+2HCl→R-CCl2-CH3 - Взаимодействие альдегидов и кетонов с PCl5, PBr5 или SF4. Рекция идёт при нагревании.
R—CHO + PCl5 → R—CHCl2, - Присоединение галогенов к алкенам
R-CH=CH2 + Cl2 → R-CHCl-CHCl - Раскрытие циклических простых эфиров при реакции с NaI в среде H3PO4+P2O5.
C4H8O + HI → I-CH2CH2CH2CH2-I
При 180 °C ТГФ с хлороводородом даёт 1,4-дихлорбутан.
Получение галогеналкенов
- С алкинами напрямую — как H-электрофилы галогеноводороды взаимодействуют медленно. Реакцию значительно ускоряют соли меди и ртути; по сути, происходит нуклеофильное присоединение галогенид-иона. Например, есть такой способ производства винилхлорида в газовой фазе на активированном угле и сулеме при 120—180 °C.
- Также и галогены присоединяются по тройной связи медленнее, чем по двойной. Вероятно, реакция идёт через КПЗ, который опять-таки является уже электрофильной частицей.
Или применяют производные алкенов. В частности, для получения того же винилхлорида есть такие два способа.
- Дегидратация этиленхлоргидрина на катализаторе.
- Дегидрохлорирование дихлорэтана в газовой фазе при 400—500 °C
Получение галогенаренов
- Галогенирование аренов или алкиларенов в ядро
Ph-H+Cl2→Ph-Cl - Разложение арендиазониевых солей
Ph-N≡N Cl→Ph-Cl
Получение бензилгалогенидов
- Галогенирование алкиларенов в боковую цепь.
Ph-CH3+Cl2→Ph-CH2Cl - Хлорметилирование
Ph-H+HCHO+HCl→Ph-CH2Cl
Просмотров: 12257
|
|