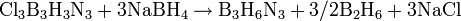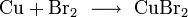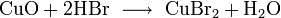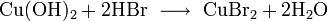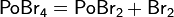Химия - Гидрид калия
28 февраля 2011Физические свойства
Гидрид калия образует бесцветные ионные кристаллы кубической сингонии с решеткой типа NaCl. Хорошо растворим в расплавленном калии, не растворяется в органических растворителях. Обладает высокой теплопроводностью.
Получение
Гидрид калия получают прямой реакцией расплавленного калия с водородом под давлением:
Эта реакция была открыта Гемфри Дэви вскоре после его открытия в 1807 году калия, когда он отметил, что металл будет испаряться в токе водорода при нагревании только ниже точки кипения.
Химические свойства
Гидрид калия является ионным соединением KH. Его расплав проводит электрический ток, при электролизе на аноде выделяется водород. С химической точки зрения гидрид калия это соль несуществующей «водородистой» кислоты.
Вещество нестабильно и при нагревании распадается на компоненты:
Гидрид калия обладает высокой химической активностью, является сильным восстановителем. Окисляется кислородом:
Взаимодействует с водой:
кислотами:
спиртами:
и газообразным аммиаком:
Взаимодействует с галогенами:
С углекислотой образует формиат калия:
Взаимодействует с оксидом кремния:
Просмотров: 2304
|
|