Химия - Гидроксид бария
28 февраля 2011Гидроксид бария — одно из сложных неорганических веществ. Является сильным основанием. Химическая формула — Ba2
Описание
Гидроксид бария при стандартных условиях представляет собой бесцветные кристаллы. Насыщенный раствор гидроксида бария называют баритовой водой. Гигроскопичен. Не растворим в спирте, но растворим в воде. Образует кристаллогидраты с одной, двумя, семью и восемью молекулами воды. Гидроксид бария токсичен, ПДК составляет 0,5 мг/м³.
Получение
1. Взаимодействие металлического бария с водой:

2. Взаимодействие оксида бария с водой:
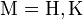
3. Взаимодейстивие сульфида бария с водой:

Химические свойства
1. Взаимодействие с кислотами с образованием соли и воды:
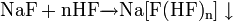
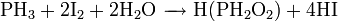
2. Взаимодействие с кислотными оксидами с образованием соли и воды:
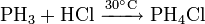

Применение
Применяют гидроксид бария как реактив на SO4 и CO3, для очистки раститительных масел и животных жиров, как компонент смазок, для удаления SO4 из промышленных растворов, получения солей бария, а также гидроксидов рубидия и цезия из их сульфатов и карбонатов.
Просмотров: 4434
|
|