Химия - Нитрат железа(III)
15 июля 2011Оглавление:
1. Нитрат железа(III)
2. Химические свойства
неорганическое химическое соединение, соль азотной кислоты и железа с формулой 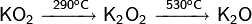 . Хорошо растворяется в воде. Из водных растворов кристаллизуется в виде нонагидрата Fe3·9H2O.
. Хорошо растворяется в воде. Из водных растворов кристаллизуется в виде нонагидрата Fe3·9H2O.
Физические свойства
Нонагидрат нитрата железа Fe3·9H2O — очень гигроскопичные светло-фиолетовые кристаллы с моноклинной решёткой. Хорошо растворяются в воде. При нагревании плавится при 50,1 °C с частичным разложением и выделением HNO3.
Гексагидрат нитрата железа Fe3·6H2O — бесцветные гигроскопичные кристаллы с кубической решёткой. Образуется при кристаллизации из раствора с содержанием HNO3 около 50%.
Безводный нитрата железа получить не удалось.
Получение
Нитрат железа получают взаимодействием железной стружки с 20-30% раствором азотной кислоты:
В производстве этот процесс проводят продувая через раствор воздух:
В лабораторной практике нитрат железа можно получить обменной реакцией:
Добавив к гидроксонитрату церия азотную кислоту и сульфат железа получим следующие продукты реакции:
Просмотров: 5536
|
|