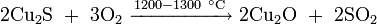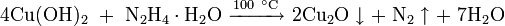Химия - Оксид никеля(II)
15 июля 2011Оглавление:
1. Оксид никеля(II)
2. Химические свойства
3. Безопасность
это неорганическое бинарное соединение двухвалентного никеля с кислородом. Химическая формула NiO. Встречается в природе в виде редкого минерала бунзенита.
Физические свойства
Оксид никеля — кристаллическое вещество, в зависимости от способа получения и термической обработки имеет цвет от светло- до тёмно-зелённого или чёрного. Имеет две кристаллические модификации:
- α-NiO до Т<252 °C, антиферромагнетик, тригональная сингония, параметры элементарной ячейки a = 0,29549 нм, c = 0,7228 нм, d = 6,67 г/см³;
- β-NiO при Т>252 °C, кубическая сингония, пространственная группа F m3m, a = 0,41768 нм, Z = 4, структура типа NaCl, d = 7,45 г/см³.
Получение
В природе оксид никеля встречается в виде минерала бунзенита — октаэдрические кристаллы, цвет от тёмно-зелёного до буровато-чёрного в зависимости от примесей. Химический состав нестехиометрический NiOx, где x = ~1 с примесями Bi, Co, As. Очень редок, встречается в Иогангеоргенштадте, в Саксонии.
Оксид никеля можно синтезировать непосредственно из элементов окислением Ni при нагревании на воздухе или в кислороде:
Оксид никеля может быть получен термическим разложением в гидроксида никеля или некоторых солей двухвалентного никеля:
Просмотров: 3411
|
|