Химия - Ортоэфиры - Синтез
28 февраля 2011Оглавление:
1. Ортоэфиры
2. Синтез
3. Нахождение в природе
Ортоэфиры могут быть синтезированы реакцией Вильямсона - взаимодействием тригалогеналканов с алкоголятами щелочных металлов:
- RCCl3 + RONa
 RC3 + NaCl
RC3 + NaCl
Для синтеза ортокарбонатов в реакции Вильямсона используется четыреххлористый углерод или хлорпикрин:
- CCl4 + RONa
 C4 + NaCl
C4 + NaCl - CCl3NO2 + 4 RONa
 C4 + 3NaCl + NaNO2
C4 + 3NaCl + NaNO2
Синтез Вильямсона ортоэфиров карбоновых кислот в случае наличия в трихлоралкане подвижных атомов водорода в α- или β- положениях может осложняться реакциями элиминирования галогеноводорода, ведущих при наличии водорода в β-положении к алкенам и, в случае наличии водорода в α-положении - карбенов.
В синтезе ортоэфиров по Вильямсону также используются простые α-галогеналкиловые эфиры: ортоформиаты с умеренными выходами могут быть получены взаимодействием 1,1-дихлордиметилового эфира с алкоголятами и фенолятами натрия:
- CH3OCHCl2 + RONa
 CH3OCHR2 + NaCl
CH3OCHR2 + NaCl
Аналогично протекает взаимодействие хлордифеноксиметана с фенолами и алифатическими спиртами, в присутствие пиридина, дающая с хорошими выходами соответствующие ортоформиаты:
- ClCH2 + ROH
 ROCH2
ROCH2
Другой метод синтеза ортоэфиров карбоновых кислот - реакция Пиннера: действие НСl на нитрилы избытке спирта; реакция идет через промежуточное образование гидрохлоридов иминоэфиров, которые могут быть выделены и использованы для получения смешанных ортоэфиров:
- R-CN + HCl
 R-C=NH
R-C=NH - R-C=NH + ROH
 R-C=NH2 Cl
R-C=NH2 Cl - R-C=NH2 Cl + 2ROH
 R-C2OR + NH4Cl
R-C2OR + NH4Cl
Ортоэфиры также синтезируются катализируемым кислотами присоединением спиртом к ацеталям кетенов:
- RRC=C2 + ROH
 RRCH-C2OR
RRCH-C2OR
Взаимодействие сложных эфиров с эпоксидами ведет к циклическим ортоэфирам, содержащим 1,3-диоксолановое кольцо:
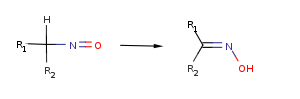
Эта реакция используется для синтеза спиро-1,3-диоксоланов:
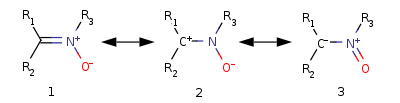
Просмотров: 3831
|
|