Химия - Реакции радикального замещения
28 февраля 2011Реакции радикального замещения — реакции замещения, в которых атаку осуществляют свободные радикалы — частицы, содержащие один или несколько неспаренных электронов.
Реакции радикального замещения обозначают SR.
Механизм радикального замещения
1. Первая стадия — инициирование цепи. Она может начаться спонтанно, фотохимически, электрохимически, посредством нагревания или путем химического иницирования.
2. Вторая стадия — развитие цепи. На этой стадии радикалы реагируют с молекулами, образуя продукты реакции и новые радикалы.
3. Третья стадия — обрыв цепи или рекомбинация свободных радикалов.
Реакции радикального замещения ускоряются в условиях генерирования свободных радикалов и замедляются в присутствии веществ, улавливающих свободные радикалы.
Типовые реакции радикального замещения
Радикальное галогенирование
Инициация галогенирования, обычно, происходит под действием облучения:
Развитие цепи:
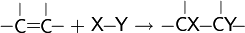
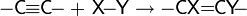
Обрыв цепи:
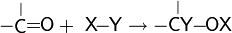
Радикальное окисление
При низких температурах в присутствии кислорода воздуха, света, а также иногда следов некоторых металлов органические соединения вступают в реакции автоокисления:
Зарождение цепи:
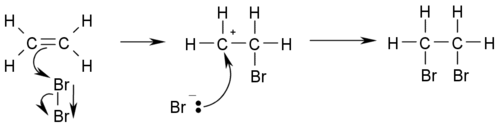
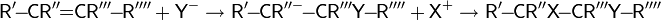
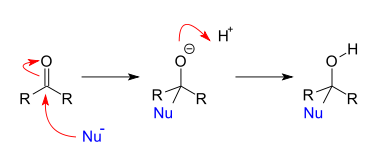
Развитие цепи:
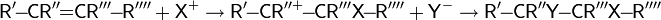
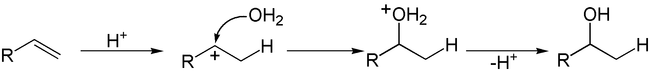
Альтернативный путь:
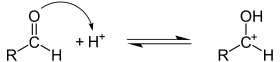
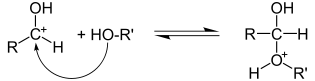
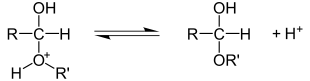
Прочие реакции радикального замещения
Реакция Бородина — Хунсдикера:
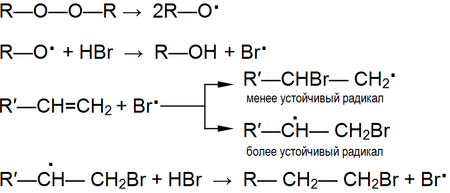
Реакция Бартона :
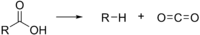
Просмотров: 3232
|
|