Химия - Стандартный электродный потенциал - Нестандартные условия
01 марта 2011Оглавление:
1. Стандартный электродный потенциал
2. Таблица стандартных электродных потенциалов
3. Нестандартные условия
Стандартные электродные потенциалы даны при стандартных условиях. Однако, реальные ячейки могут действовать и при нестандартных условиях. При данном стандартном потенциале, потенциал при нестандартных эффективных концентрациях может быть вычислен с использованием уравнения Нернста:
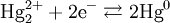
Величины E зависят от температуры и обычно относятся к стандартному водородному электроду при этой температуре. Для конденсированных фаз, величины потенциалов также зависят от давления.
Просмотров: 5563
|
|