Химия - Сульфат меди(II) - Свойства
15 июля 2011Оглавление:
1. Сульфат меди(II)
2. Получение
3. Свойства
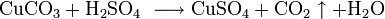
При нагревании последовательно отщепляет две молекулы воды, переходя в тригидрат CuSO4 · 3H2O, затем в моногидрат CuSO4 · H2O, и выше 258 °C образуется безводная соль. Термическое разложение становится заметным выше 650 °C:
Растворимость сульфата меди по мере роста температуры проходит через плоский максимум
Как и все соли, образованные ионами слабого основания и сильной кислоты, сульфат меди гидролизуется, и даёт кислую среду. Константа диссоциации составляет 5×10.
С сульфатами щелочных металлов и аммония образует комплексные соли, например, Na2·6H2O.
Окрашивает огонь в зелёный цвет.
Применение


Сульфат меди наиболее важная соль меди, часто служит исходным сырьём для получения других соединений.
Безводный сульфат меди можно использовать как индикатор влажности, с его помощью в лаборатории проводят осушку этанола и некоторых других веществ.
Наибольшее количество непосредственно применяемого CuSO4 расходуется на борьбу с вредителями в сельском хозяйстве, в составе бордосской смеси с известковым молоком — от грибковых заболеваний и виноградной тли.
В строительстве водный раствор сульфата меди применяется для нейтрализации последствий протечек, ликвидации пятен ржавчины, а также для удаления выделений солей с кирпичных, бетонных и оштукатуренных поверхностей; а также как средство для предотвращения гниения древесины.
Также он применяется для изготовления минеральных красок, в медицине, как один из компонентов электролитических ванн для меднения и т. п. и как часть прядильных растворов в производстве ацетатного волокна.
В пищевой промышленности зарегистрирован в качестве пищевой добавки E519.
В пунктах скупки лома цветных металлов раствор медного купороса применяется для выявления цинка, марганца и магния в алюминиевых сплавах и нержавейке. При выявлении этих металлов появляются красные пятна.
Просмотров: 8419
|
|