Химия - Тепловой эффект химической реакции - Температурная зависимость теплового эффекта реакции
01 марта 2011Оглавление:
1. Тепловой эффект химической реакции
2. Стандартная энтальпия образования
3. Температурная зависимость теплового эффекта реакции
4. Стандартная энтальпия растворения
5. Стандартная энтальпия нейтрализации
Чтобы рассчитать температурную зависимость энтальпии реакции, необходимо знать мольные теплоемкости веществ, участвующих в реакции. Изменение энтальпии реакции при увеличении температуры от Т1 до Т2 рассчитывают по закону Кирхгофа:
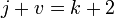
Если в данном интервале температур происходят фазовые превращения, то при расчёте необходимо учесть теплоты соответствующих превращений, а также изменение температурной зависимости теплоемкости веществ, претерпевших такие превращения:
где ΔCp — изменение теплоемкости в интервале температур от Т1 до температуры фазового перехода; ΔCp — изменение теплоемкости в интервале температур от температуры фазового перехода до конечной температуры, и Tf — температура фазового перехода.
Стандартная энтальпия сгорания
ΔHгор, тепловой эффект реакции сгорания одного моля вещества в кислороде до образования оксидов в высшей степени окисления. Теплота сгорания негорючих веществ принимается равной нулю.
Просмотров: 4442
|
|