Химия - Триметилхлорсилан - Применение
01 марта 2011Оглавление:
1. Триметилхлорсилан
2. Применение
3. Безопасность
- Триметилхлорсилан широко используется в органическом синтезе как источник триметилсилильной группы, так и безводный источник хлорида. Функциональные группы спиртов и аминов легко поддаются реакции с триметилхлорсиланом, образуя триметилсилильные эфиры или триметилсилильные амины. Полученные группы могут быть использованы как защитные группы
- однако лабильность триметилсиланового фрагмента ограничивает такое их применение. Так триметилсилильная группа может быть снята фторид ионом из-за высокого сродства кремния к фтору
- Триметилсилирование увеличивает летучесть вещества, что используется в газовой хроматографии при анализе таких нелетучих веществ, как глюкоза
- Триметилхлорсилан реагирует с ацетиленидами металлов, образуя триметилсилилалкины, которые являются защищённой формой алкинов.
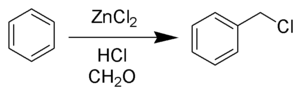
- Триметилхлорсилан реагирует со спиртами с образованием хлороводорода, что может быть использовано для получения безводных растворов хлороводорода в спирте — что, в свою очередь, может быть использовано в получении в мягких условиях сложных эфиров из карбоновых кислот и кеталей из кетонов.
- В присутствии триэтиламина или диизопропиламида лития енолизируемые альдегиды, кетоны и сложные эфиры превращаются в триметилсилильные эфиры енолов:
-
-
 : :
: :
-
Несмотря на их гидролитическую нестабильность этих веществ, они нашли широкое применение в органической химии. Окисление двойной связи эпоксидированием таких силилированных енолов с дальнейшим гидролизом может быть использовано для введения гидроксигруппы в α-положение к карбонильной группе. Триметилсилиловые эфиры енолов могут также быть использованы в качестве эквивалента енола в конденсации Мукайямы альдольной конденсации.
- Триметилхлорсилан спользуется для С-силилирования карбанионов, реактивов Гриньяра и литийорганических соединений, за счет индуктивного эффекта такие силилированные соединения с атомом водорода в α-положении приобретают свойства CH-кислот. Присоединение стабилизированных триметилсилильной группой α-карбанионов к карбонильным соединениям ведет к образованию β-гидроксисиланов и дальнейшему элиминированию триметилсиланола с образованием алкена:
В случае электронакцепторных заместителей в α-триметилсилильном карбанионе реакция идет по механизму, близкому к реакции Виттига и протекает стереоселективно. Этот метод используется для синтеза алкенов из карбонильных соединений.
Просмотров: 3742
|
|