Химия - Цинкаты
28 февраля 2011Оглавление:
1. Цинкаты
2. Номенклатура неорганических соединений
соединения, содержащие комплексный анион; группа веществ теоретических оксо- и гидроксоцинкат анионов. Соединения образуются при соединении амфотерного гидроксида цинка в избытке щелочи. Цинкаты щелочных металлов получают растворением цинка, его окиси или гидроокиси в растворах или расплавах щелочей. Они растворимы в воде и кристаллизуются из растворов. Цинкаты других металлов получают сплавлением ZnO с соответствующими окислами. В воде практически нерастворимы.
В химии к цинкатам могут относиться:
- Соли, содержащие Zn4, также называемые тетрагидроксоцинкат-ионами. Например, цинкат кальция CaZn4·2H2O или Na2Zn4 или полимерный анион, например NaZn3·H2O.
- Щелочные растворы, приготовленные из металлического цинка, гидроокиси цинка и оксида цинка, которые содержат различные виды анионов, например, Zn4. Такие соединения используются в промышленности.
- Оксиды, содержащие цинк и менее электроотрицательный элемент, например Na2ZnO2.
Виды анионов
| Анион | Кислота |
|---|---|
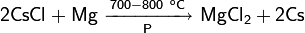 |
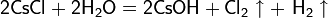 |
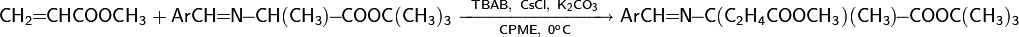 |
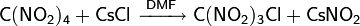 |
 |
 |
 |
 |
 |
 |
Просмотров: 3702
|
|