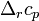Химия - Закон Кирхгофа (химия)
06 мая 2011Закон Кирхгофа гласит, что температурный коэффициент теплового эффекта химической реакции равен изменению теплоёмкости системы в ходе реакции. Уравнение Кирхгофа, являющееся следствием этого закона используется для расчёта тепловых эффектов при разных температурах.
Дифференциальная форма закона:
Интегральная форма закона:
где Cp и CV — изобарная и изохорная теплоёмкости, 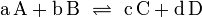 — разность изобарных теплоёмкостей продуктов реакции и исходных веществ,
— разность изобарных теплоёмкостей продуктов реакции и исходных веществ, 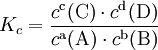 — разность изохорных теплоёмкостей продуктов реакции и исходных веществ, а ΔrH и ΔrU — соответствующие тепловые эффекты.
— разность изохорных теплоёмкостей продуктов реакции и исходных веществ, а ΔrH и ΔrU — соответствующие тепловые эффекты.
Если разница 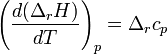 невелика, то можно принять
невелика, то можно принять 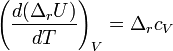 и
и 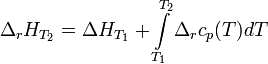 , соответственно интегральная форма уравнений примет следующий вид:
, соответственно интегральная форма уравнений примет следующий вид:
При большой разнице температур необходимо учитывать температурные зависимости теплоёмкостей: 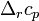 и
и 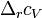
Просмотров: 5022
|
|