Химия - Законы Коновалова - Второй закон Коновалова
01 марта 2011Оглавление:
1. Законы Коновалова
2. Второй закон Коновалова
Второй закон Коновалова описывает растворы с отклонениями от свойств идеальных растворов и объясняет существование азеотропных растворов, состав которых при перегонке не изменяется:
- Экстремумы на кривых полного давления пара отвечают такому равновесию раствора и насыщенного пара, при котором состав обеих фаз одинаков

Доказательство второго закона Коновалова
Согласно уравнению Дюгема-Маргулеса, которое описывает равновесие в идеальных бинарных растворах газов или давление насыщенного пара над идеальным бинарным жидким раствором
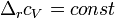 или
или 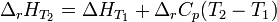
, где 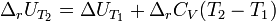 — мольная доля второго компонента в растворе,
— мольная доля второго компонента в растворе, 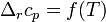 и
и 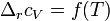 — парциальные давления первого и второго компонента.
— парциальные давления первого и второго компонента.
Отсюда следует, что

По закону Дальтона


где 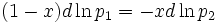 и
и 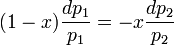 — мольные доли первого и второго компонента в насыщенном паре,
— мольные доли первого и второго компонента в насыщенном паре, 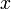 — общее давление в системе. Тогда
— общее давление в системе. Тогда 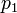
Поскольку общее давление есть сумма парциальных, то 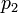 . Подставив в это выражение значение
. Подставив в это выражение значение 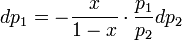 из предыдущего получим
из предыдущего получим
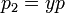
Разделив обе части на 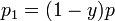 и раскрыв скобки получим, что
и раскрыв скобки получим, что
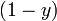
В экстремуме 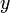 , следовательно
, следовательно
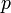
Поскольку 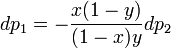 , так как с ростом концентрации второго компонента растёт и его парциальное давление, то равенство может соблюдаться только если
, так как с ростом концентрации второго компонента растёт и его парциальное давление, то равенство может соблюдаться только если 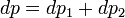 — когда состав пара и раствора одинаков, что и доказывает второй закон Коновалова. Растворы, состав которых отвечает точке экстремума, кипят при постоянной температуре, а их состав при перегонке не изменяется. Такие растворы называются «азеотропными растворами» или «азеотропами». Разделение азеотропов методом фракционной перегонки невозможно. Для разделения таких растворов используют химические методы, перегонку с третьим компонентом либо фракционную перегонку при другом давлении.
— когда состав пара и раствора одинаков, что и доказывает второй закон Коновалова. Растворы, состав которых отвечает точке экстремума, кипят при постоянной температуре, а их состав при перегонке не изменяется. Такие растворы называются «азеотропными растворами» или «азеотропами». Разделение азеотропов методом фракционной перегонки невозможно. Для разделения таких растворов используют химические методы, перегонку с третьим компонентом либо фракционную перегонку при другом давлении.
Просмотров: 7968
|
|