Химия - Актиноиды - Получение
28 февраля 2011Оглавление:
1. Актиноиды
2. Изотопы
3. Распространение в природе
4. Получение
5. Cвойства
6. Соединения
7. Применение
8. Токсичность
9. Галерея изображений

В большинстве случаев для получения чистого вещества элементов применяют разложение химического соединения этого элемента, обычно путём реакции его оксида, фторида и т. д. с водородом. Однако этот метод неприменим к актиноидам, поскольку они встречаются очень редко в природе, и поэтому для их выделения применяются более сложные методы очистки соединений, а затем и получения элементов данной группы.
Чаще всего для выделения чистых соединений актиноидов используют фториды, поскольку они плохо растворяются в воде и могут быть легче удалены путём обменной реакции. Фториды актиноидов восстанавливают кальцием, магнием или барием, так как они сравнительно более активны по сравнению с третьей и последующими подгруппами. Например, металлический америций добывают действием на его трифторид парами бора:
Аналогично добывают и остальные. Плутоний выделяют из его тетрафторида, восстанавливая его:
Металлический уран также добывают из тетрафторида, но в качестве восстановителя используют магний:
Среди актиноидов наиболее легко добываются торий и уран. Торий добывают преимущественно из монацита. При этом дифосфат тория2) с примесями редкоземельных элементов, которые осаждаются при повышенном pH сульфатного раствора, обрабатывают азотной кислотой, а нитрат тория экстрагируют трибутилфосфатом. Ещё лучше из кислых растворов торий отделяется от РЗЭ в присутствии роданид-ионов.
При переработке монацита разложением 45%-ого раствора гидроксида натрия сначала добывают гидроксиды смешанных металлов, которые затем отфильтровывают, промывают водой и растворяют в концентрированной хлорной кислоте. Далее кислый раствор нейтрализуют гидроксидами до pH=5,8. При этом оседает гидроксид тория4) с примесями гидроксидов редкоземельных элементов, основная масса которых остается в растворе.
Гидроксид тория растворяют в неорганической кислоте и снова очищают от редкоземельных элементов. Более эффективным считается метод растворения гидроксида тория в азотной кислоте, потому что добытый раствор можно очистить посредством экстракции органическими растворителями:
Но в нитратной кислоте ториевый концентрат не полностью растворяется. В хлороводороде он растворяется лучше, образуя хлорид тория и воду.

Можно отделить торий от редкоземельных элементов осаждением оксалата тория из кислых растворов. Но самым перспективным считается метод экстрагирования солей тория органическими растворителями, которые не смешиваются с водой.
Металлический торий отделяют из безводного оксида, хлорида или фторида с помощью кальция в инертной атмосфере:
 .
.
Иногда торий добывают электролизом нагретого фторида в смеси хлоридов натрия и калия. Электролиз проводят при 700—800 °С в графитовом тигле. Очень чистый торий добывают разложением его йодида с помощью метода Ван Аркеля и де Бура.
Уран добывают из его руд разными способами. Сначала руду поджигают, затем воздействуют на неё кислотами, чтобы уран перешёл в растворённое состояние. При использовании серной кислоты, которая растворяет лишь соединения шестивалентного урана, нужно добавлять ещё и оксиды, чтобы перевести четырёхвалентный уран в шестивалентный. На следующей стадии уран отделяют из примесей. Для этого раствор отфильтровывают, а иногда непосредственно с пульпы экстрагируют соли урана органическими растворителями. Из нитратного раствора лучше всего экстрагировать уран в керосиновом растворе ТБФ. При этом в органическую фазу переходит комплекс — UO22·2ТБФ.
Когда раствор, который состоит из солей урана, отфильтрован от нерастворимого осадка, уран можно выделить осаждением гидроксидами2U2O7) или пероксидом водорода.
Если в урановой руде присутствует примесь таких минералов, как доломит, магнезит и т. п., а они при действии кислоты на урановую руду нейтрализуют большое количество кислоты, целесообразнее использовать карбонатный способ разложения урановой руды. Основным реагентом для этого является водный раствор соды, который переводит уран в растворимое комплексное соединение —. Данное соединение является стабильным в водных растворах при невысоких концентрациях гидроксид-ионов. Использование карбоната натрия имеет преимущество, потому что при его использовании, кроме урана, практически все другие металлы остаются в виде осадка. Преимущество карбонатного способа разложения урановых руд относительно кислотного состоит в отсутствии коррозийных характеристик рабочих растворов. Недостатком этого способа является то, что в присутствии карбоната натрия соединения четырёхвалентного урана не растворяются. Поэтому для полного очищения урана руду обрабатывают содой при нагревании и единовременной подачи под давлением кислорода:
 .
.
Из данного уравнения видно, что наилучшим растворителем урана при карбонатной переработке является смесь карбоната с его бикарбонатом. Когда берется средний карбонат, то из-за высокого pH раствора часть урана может выпасть в осадок в виде диураната. Из карбонатных растворов диуранат выделяют, восстанавливая его водородом в присутствии никеля. При этом получается нерастворимый тетракарбонат урана.
Перспективным является также способ с использованием высокополимерных смол в качестве полиэлектролитов. В смолах происходит обмен ионов, в результате чего выделяется уран. С помощью данного способа можно выделить уран как из кислых, так и из основных растворов. Поскольку, по сравнению с остальными трансурановыми металлами, уран легче создает анионные комплексы, например,, то при выделении в реакции ионного обмена урана лучше пользоваться анионитами с четвертинными аммонийными группами R4NA.
Из анионита уран вымывают раствором нитрата аммония или азотной кислоты.
После разделения уран выделяют в виде нитрата уранила — UO22·6H2O. Из него при нагревании получится оксид урана, который при восстановлении водородом переходит в диоксид:
При действии фтороводорода на диоксид урана добывают тетрафторид урана, который потом можно восстановить магнием до металлического урана:
Для выделения плутония из продуктов расщепления радиоактивных материалов облученный нейтронами уран растворяют в азотной кислоте. К полученному раствору добавляют восстановитель, который переводит плутоний из степени окисления +6 в +4, а уран остается в виде нитрата уранила2). После обработки восстановителем раствор нейтрализуют карбонатом аммония до pH=8. При этом Pu переходит в осадок.
Можно воспользоваться и другим методом. После восстановления нитратного раствора газообразной серой добавляют плавиковую кислоту и осаждают ионы лантана, а вместе с этим осаждаются и фториды плутония и нептуния. После фильтрования и промывания осадок фторидов обрабатывают броматом калия для окисления нептуния до 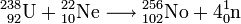 , который переходит в раствор. Далее с помощью более сильных окислителей переводят плутоний в Pu и тем самым отделяют его от лантаноидов.
, который переходит в раствор. Далее с помощью более сильных окислителей переводят плутоний в Pu и тем самым отделяют его от лантаноидов.
Часто для разделения плутония и других актиноидов, начиная с урана, пользуются экстракцией трибутилфосфатом. Сначала экстрагируют нитраты Pu и U, а потом экстрагент приводят в контакт с гидразином и вымывают восстановленный плутоний.
Препараты, содержащие актиний, бывают загрязнены РЗЭ. Сложность очистки актиния осложняется сходством актиния и лантана, что осложняет отделение актиния. Актиний можно получить несколькими способами — ядерными реакциями или методами отделения, осаждения или ионного обмена. В первом случае применяется ядерная реакция с участием изотопов радия. Во втором случае применяются химические методы получения актиния — реакции ионного обмена, очистка от примесей с помощью реакций. Существует, помимо вышеописанных методов отделения актиния от примесей, и методы хроматографии, методы экстракции, электрохимии и другие способы, также применимые к остальным актинидам.
Просмотров: 20602
|
|