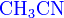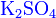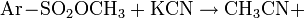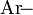Химия - Нитрилы - Способы получения
28 февраля 2011Оглавление:
1. Нитрилы
2. Химические свойства
3. Способы получения
4. Анализ, применение и токсическое действие
1. Дегидратация амидов RCONH2, аммониевых солей карбоновых кислот RCOONH4 или альдоксимов RCH=NOH при нагреве с Р2O5, PCl5, POCl3 или SOCl2. В промышленности реакцию обычно проводят в присутствии катализаторов дегидратации в атмосфере NH3, например:
2. Алкилирование синильной кислоты или её солей:
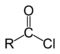
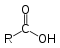
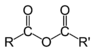
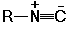 C2H5CN
C2H5CN  KI;
KI;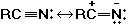
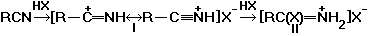

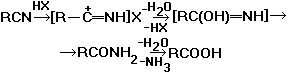 ;
;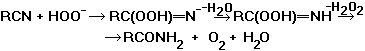
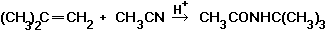 где
где 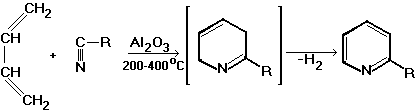 ароматический радикал.
ароматический радикал.
При алкилировании алкил- и аралкилгалогенидами широко применяют межфазный катализ, например при промышленном получении бензилцианида. Ароматические нитрилы получают взаимодействием арилгалогенидов с CuCN, сплавлением солей сульфокислот с NaCN или разложением диазосоединений в присутствии CuCN, например:
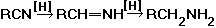 где
где 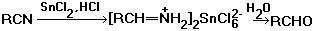 фенил радикал
фенил радикал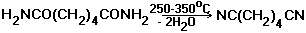

Взаимодействие ароматических углеводородов с хлорцианом в присутствии хлорида алюминия:
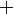

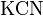
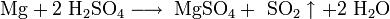
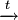

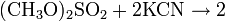 .
.
3. Присоединение HCN по кратным связям, например:
Циангидрины получают присоединением HCN к карбонильным соединениям или эпоксидам в присутствии оснований.
4. Окисление углеводородов, спиртов и альдегидов. Совместное окисление углеводородов и NH3 кислородом воздуха при 400—500 °C в присутствии молибдатов и фосфомолибдатов Bi, молибдатов и вольфраматов Те и Се и других катализаторов: Для окисления могут быть использованы спирты в альдегиды, например:
- CH2=CHCH3 + NH3 + O2 → CH2=CHCN + H2O;
Для окисления могут быть использованы спирты и альдегиды, например:
- C2H5OH + NH3 + → CH3CN + H2O + H2;
Нитрилы образуются также при действии окислителей на амины:
- Ph-CH2NH2 → PhCN + 2H2;
5. Теломеризация олефинов с галогенцианидами или реакций последних с магнийорганическими соединениями:
nCH2=CH2 + ClCN → ClnCN; RMgX + ClCN → RCN + MgXCl;
Просмотров: 7656
|
|