Химия - Оксид молибдена(VI)
15 июля 2011Оглавление:
1. Оксид молибдена(VI)
2. Применение
Оксид молибдена — бинарное неорганическое химическое соединение кислорода с молибденом. Химическая формула 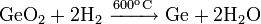 . Это соединение производится в крупных масштабах из любого соединения молибдена. Это соединение используется в качестве сырья для производства металлического молибдена.
. Это соединение производится в крупных масштабах из любого соединения молибдена. Это соединение используется в качестве сырья для производства металлического молибдена.
Степень окисления молибдена в этом соединении равна +6.
Структура
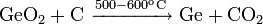
В газовой фазе, три атома кислорода вместе связаны с центральным атомом молибдена. В твердом состоянии безводный 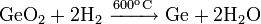 состоит из слоев искаженных октаэдров
состоит из слоев искаженных октаэдров  в ромбической форме кристаллов. Края октаэдров образуют цепочки, которые соединены с атомами кислорода, которые и образуют слои. Октаэдры имеют один короткую связь O—Mo с несоединенным кислородом.
в ромбической форме кристаллов. Края октаэдров образуют цепочки, которые соединены с атомами кислорода, которые и образуют слои. Октаэдры имеют один короткую связь O—Mo с несоединенным кислородом.
Свойства и получение
Слабо парамагнитные двулучепреломляющие белые орторомбические кристаллы слоистой структуры, желтеющие при нагревании. Реагирует с кислотами, щелочами, раствором аммиака и сульфида натрия. Растворяется в воде, в избытке растворов щелочей или карбонатов щелочных металлов. Триоксид молибдена производится промышленным методом обжига дисульфида молибдена — главной руды молибдена:
- 2MoS2 + 7O2 → 2MoO3 + 4SO2
Получается прокаливанием молибдена на воздухе при высокой температуре:
Лабораторный синтез предполагает подкисление водного раствора молибдата натрия с хлорной кислотой. При этом получаются диаква-триоксид молибдена и перхлорат натрия:
- Na2MoO4 + 2HClO4 + H2O → MoO32 + 2NaClO4
Диаква-триоксид молибдена легко теряет воду, давая моногидрат. Оба ярко-желтого цвета.
Молибденовый ангидрид растворяется в воде давая «молибденовую кислоту» H2O).
Просмотров: 3651
|
|