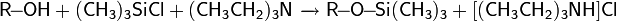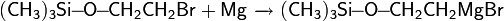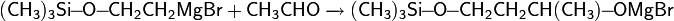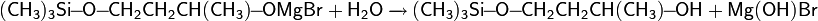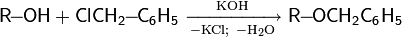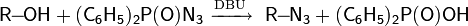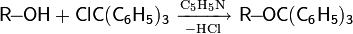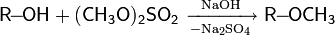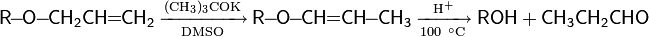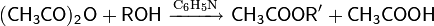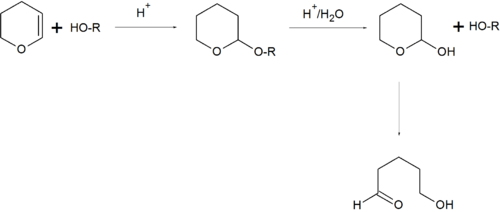Химия - Спирты - Идентификация спиртов
28 февраля 2011Оглавление:
1. Спирты
2. Классификация спиртов
3. История открытия спиртов
4. Нахождение в природе
5. Физиологическая роль спиртов
6. Физиологическое действие и токсичность спиртов
7. Физические свойства и строение спиртов
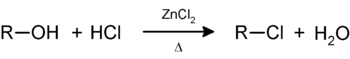
8. Получение спиртов
9. Химические свойства спиртов
10. Идентификация спиртов
11. Применение спиртов
12. Перечень используемых в статье таблиц
13. Комментарии
Химические методы идентификации спиртов
Качественный анализ гидроксильных групп
Существует множество относительно простых тестов, позволяющих выявить в органическом соединении наличие гидроксильного фрагмента, однако все они имеют довольно ограниченное применение и не являются универсальными: часто присутствие прочих функциональных групп или кратных связей в веществе могут либо не проявить искомые свойства спирта, либо дать ложно положительный эффект на ту или иную реакцию.

Приведём примеры наиболее известных качественных реакций на спирты:
- Проба Лукаса: при реакции вторичного или третичного спирта при комнатной температуре с реактивом Лукаса происходит образование галогенопроизводного, которое распознаётся по образованию характерного масла, образующего отдельную от исходного спирта фазу. При этом зафиксировав время реакции, можно различить вторичные и третичные спирты.
- Некоторые первичные спирты, например: аллиловый или бензиловый, дают положительную реакцию с реактивом Лукаса.
- Иодоформная проба: предназначена для идентификации спиртов вида R−CH−CH3 и кетонов вида R−C−CH3.
- Идентификацию спиртов осуществляют по характерному жёлтому осадку иодоформа, обладающего специфическим запахом.
- Тест Виктора Мейера : позволяет дифференцировать первичные, вторичные и третичные спирты по реакции получаемых из них нитропроизводных с азотистой кислотой. На первой стадии спирты трансформируются в галогенопроизводные, которые, в свою очередь, превращаются в нитроалканы:
- Далее взаимодействие с HNO2 делает возможными три варианта развития событий:
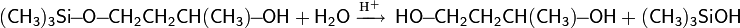
- раствор окрашивается в красный цвет=NONa)
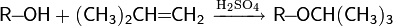
- раствор окрашивается в синий цвет
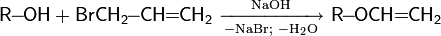
- раствор остаётся бесцветным
- Цератная проба: при взаимодействии спиртов с азотнокислым раствором гексанитратоцерата аммония, имеющим жёлтую окраску, образуются переходные комплексы красного цвета, которые затем обесцвечиваются вследствие окисления спирта и перехода Ce в анион Ce. Для спиртов, нерастворимых в воде, используют растворы в диоксане или ацетонитриле.
- Окислительная проба: при взаимодействии первичных или вторичных спиртов с реактивом Джонса в серной кислоте), имеющим оранжевую окраску, образуются продукты окисления, а сам реактив меняет цвет на зелёный или голубой благодаря солям восстановленного хрома. Важной особенностью теста является время фиксации изменения окраски — 2 секунды, по истечении которого любые дальнейшие изменения в структуре или цвете раствора не принимаются во внимание.
- Сульфидная проба: вторичные спирты при нагревании с серой образуют сероводород, который идентифицируется по образованию чёрного осадка с ацетатом свинца:
Реагенты для химической идентификации спиртов
Идентификацию конкретного спирта осуществляют по его производным, образующимся в результате его химического взаимодействия с различными реагентами: измеряя основные физические параметры получившегося производного можно c различной степенью достоверности подтвердить формулу исходного соединения.
Таблица 15. Перечень основных реагентов и образующихся производных при идентификации спиртов.
| Реагент для идентификации | Исследуемое производное спирта | Примеры идентифицируемых спиртов |
|---|---|---|
| фенилизоцианат, C6H5N=C=O | C6H5NHCOOR | этанол, аллиловый спирт, циклогексанол |
| 1-нафтилизоцианат, C10H7N=C=O | C10H7NHCOOR | пропанол-2, 2,3-диметил-2-бутанол, мирициловый спирт |
| 4-бифенилизоцианат, C6H5−C6H4N=C=O | C6H5−C6H4NHCOOR | 2,4-диметил-1-пентанол, 2-этил-1-пентанол |
| 4-нитробензоил хлорид, O2NC6H4COCl | O2NC6H4COOR | пентанол-1, трихлорэтанол, циннамиловый спирт |
| 3,5-динитробензоил хлорид, 2C6H4COCl | O2NC6H3COOR | пентанол-2, 2-хлорпропанол-1, бензиловый спирт |
| фталевый ангидрид, C6H42O | C6H4COOR | гептанол, терпинеол |
| 3-нитрофталевый ангидрид, O2NC6H32O | O2NC6H3COOR | 2-метоксиэтанол, гексанол, 2-фенилэтанол |
| псевдосахарина хлорид, C6H4 | C6H4 | метанол, бутанол, деканол |
| циануровая кислота, 3 | H2NCONHCOOR | 2-метил-2-пентанол, 5-нонанол |
Количественный анализ спиртов
Для количественного анализа спиртов, обычно, используют методы, основанные на реакции этерификации, реже — на определении активного водорода. Для гликолей также применим окислительно-восстановительный метод, где в качестве окислителя используется иодная кислота.
Для этерификации чаще всего применяют уксусный и фталевый ангидриды, а также пиромеллитовый диангидрид. Содержание спирта определяется титрованием образующейся в результате реакции кислоты гидроксидом натрия. В случае гликолей анализ проводят по реакции образующейся иодноватой кислоты с иодидом калия и последующим титрованием выделившегося иода тиосульфатом натрия:
Наконец, анализ на определении активного водорода сводится к анализу выделившегося в ходе реакции метана.
Спектральные методы анализа спиртов
Масс-спектрометрические методы анализа спиртов
Масс-спектры алифатических спиртов имеют слабые M сигналы, а для высших и сильноразветвлённых соединений практически отсутствуют, поэтому для алканолов рассматривают характеристические распады с образованием оксониевых ионов или элиминирование с образованием алкенов.
Для первичных спиртов — m/z 31, для вторичных — m/z 45, 59, 73 …, для третичных — m/z 59, 73, 87 …
Характеристические пики, связанные с элиминированием воды и алкена:,,…
ИК-спектроскопические методы анализа спиртов
ИК-спектры спиртов характеризуются двумя типами интенсивных характеристических полос поглощения:
- полосы поглощения, связанные с валентными колебаниями O−H группы: 3650—3200 см;
- полосы поглощения, связанные с валентными колебаниями С−O−H группы: 1210—1000 см.
Также выделяют полосы поглощения средней интенсивности, как правило не имеющие определяющего значения: в диапазоне 1450—1250 см и 750—650 см.
Таблица 16. Типичные полосы поглощения в инфракрасных спектрах спиртов.
| Типы связей и колебания | Диапазон, см | Описание полосы поглощения |
|---|---|---|
| O−H, валентные колебания | ||
| ROH, неассоциированные | 3650—3580 | Узкая полоса, наблюдаемая в разбавленных растворах или парах |
| ROH•••HOR, димеры | 3550—3400 | Широкая полоса, теряющая интенсивность при разбавлении |
| ROH•••HOR•••, полимеры | 3400—3200 | Широкая полоса или ряд полос |
| С−O, валентные колебания | ||
| R3COH, третичные спирты | 1210—1100 | Полосы высокой интенсивности, уменьшающейся при разбавлении |
| R2CHOH, вторичные спирты | 1125—1000 | |
| RCH2OH, первичные спирты | 1075—1000 | |
| O−H, деформационные колебания | ||
| ROH | 1450—1250 750—650 |
Широкие полосы средней интенсивности, не имеющие практического значения |
При анализе ИК-спектров необходимо учитывать, что некоторые функциональные группы дают характеристические полосы в диапазонах, близких или совпадающих с диапазонами спиртов: валентные колебания O−H группы сходны с валентными колебаниями связей N-H, C-H алкинов и воды; валентные колебания связи C−O сходны с валентными колебаниями связей C−F, C−N, N−O, P−O, C=S, S=O, P=O, Si−O, Si-H.
ЯМР-спектроскопические методы анализа спиртов
ЯМР-спектроскопические методы для ядер H широко используются для анализа спиртов, однако на положение сигнала существенно влияет природа растворителя и другие внешние факторы, поэтому величины характеристических сдвигов протонов рассматривают либо для чистых веществ, либо для их растворов в диметилсульфоксиде или трихлордейтерометане. Для алифатических и алициклических спиртов δ: 0,5—3,0.
Химические сдвиги ядер С в спиртах составляют диапазон 50—100.
Также для изучения гидроксильных соединений применяют импульсную Фурье-спектроскопию на ядрах O. Значительная разница в сдвигах для первичных, вторичных и третичных спиртов относительно воды H2O позволяет установить или подтвердить структуру исследуемого соединения.
Просмотров: 148037
|
|